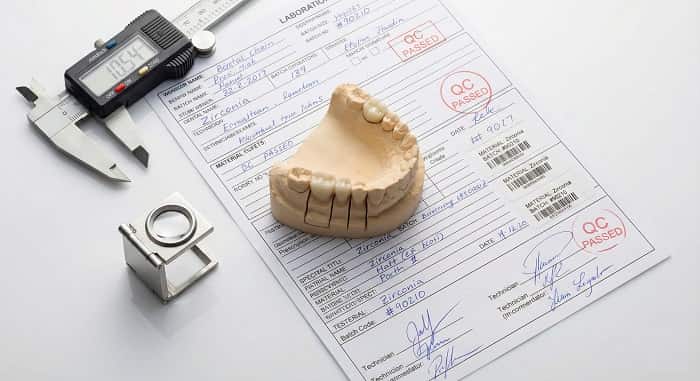
استانداردهای مستندسازی در لابراتوار دندانسازی اگر در یک لابراتوار شلوغ دندانسازی کار کرده باشید میدانید بدترین جملهای که میتوان شنید این است: «این کیس را کی ساخته؟ با چه مادهای بوده؟ نسخهاش کجاست؟». در چنین لحظههایی است که نبود استانداردهای مستندسازی در لابراتوار دندانسازی خودش را نشان میدهد؛ وقتی هیچکس دقیقا نمیداند چه مسیری طی شده و چطور باید مشکل را ردیابی و اصلاح کرد.
در نگاه امروز به لابراتوار دندانی، مستندسازی فقط «بایگانی کاغذها» نیست؛ بخش جدی سیستم مدیریت کیفیت، الزامات قانونی تجهیزات پزشکی و پایه تصمیمگیری در کنترلکیفی و نهاییسازی (QC) است. استانداردهایی مثل ایزو ۱۳۴۸۵ (ISO 13485)، طرح «داماس» (DAMAS) و مقررات تجهیزات پزشکی اروپا یا MDR، همگی روی وجود پرونده فنی، ردیابی مواد و ثبت سیستماتیک کنترلها تأکید میکنند.
در این مقاله، گامبهگام میبینیم استانداردهای مستندسازی در لابراتوار دندانسازی چه اجزایی دارند، چه نسبتی با QC پیدا میکنند و چطور میتوانید آنها را بهصورت عملی در لابراتوار خود پیاده کنید.
جایگاه استانداردهای مستندسازی در مدیریت لابراتوار دندانسازی
اولین کارکرد استانداردهای مستندسازی در لابراتوار دندانسازی این است که کیفیت را از سطح سلیقه فردی به سطح سیستم قابلپیگیری ارتقا میدهد. وقتی برای هر کیس، هر ماده و هر مرحله تولید، سند مشخصی وجود داشته باشد، لابراتوار میتواند:
- کیفیت پروتزها را اندازهگیری و مقایسه کند
- علت خطاها و ریمیکها را دقیقتر شناسایی کند
- در برابر دندانپزشک، بیمار و نهادهای نظارتی پاسخگو باشد
در چارچوب مقررات MDR اروپا برای وسایل سفارشی دندانی، هر پروتز باید «اظهارنامه انطباق» و یک «پرونده فنی» داشته باشد؛ یعنی مجموعهای از اسناد طراحی، مواد، فرایند تولید و نتایج کنترلکیفی که نشان دهد دستگاه با الزامات ایمنی و عملکردی سازگار است.
از طرف دیگر، استانداردهای کیفیت مانند ایزو ۱۳۴۸۵ (ISO 13485) برای سیستم مدیریت کیفیت تجهیزات پزشکی، مستندسازی کامل فرایندها، ریسکها، سوابق تولید و شکایات را جزو الزامات خود میدانند. به زبان ساده، بدون مستندات منظم، عملا مدیریت کیفیت پایدار ممکن نیست.
چارچوبهای بینالمللی مرتبط با مستندسازی در لابراتوار دندانسازی
برای اینکه استانداردهای مستندسازی در لابراتوار دندانسازی را درست طراحی کنید، لازم است بدانید دنیا از شما چه میخواهد؛ حتی اگر هنوز الزام حقوقی مستقیم نداشته باشید.
ایزو ۱۳۴۸۵ (ISO 13485) بهعنوان استاندارد سیستم مدیریت کیفیت تجهیزات پزشکی، روی چند محور تمرکز دارد: مستندات فرایند، ردیابی مواد، کنترل تغییرات، سوابق آموزش و اسناد کنترلکیفی. بسیاری از لابراتوارهایی که در بازارهای بینالمللی فعالاند، این استاندارد را بهعنوان معیار اعتماد به کار میگیرند
طرح «داماس» (Dental Appliance Manufacturers Audit Scheme یا DAMAS) یک سیستم مدیریت کیفیت مخصوص لابراتوارهای دندانی است که بهطور ویژه بر روی مستندسازی، ردیابی، کنترل تجهیزات و آموزش کارکنان تمرکز دارد و بهصورت دورهای توسط ممیز مستقل پایش میشود
در سطح اروپا، مقررات MDR لابراتوار را بهعنوان «تولیدکننده وسیله پزشکی سفارشی» میبیند و وجود پرونده فنی، سیستم مدیریت کیفیت و مستندات ریسک و عملکرد را الزامی میکند.
جمعبندی این چارچوبها این است که استانداردهای مستندسازی نه یک کار تزئینی، بلکه ستون قانونی و حرفهای کار لابراتوار است.
اجزای اصلی سیستم مستندسازی استاندارد در لابراتوار
برای پیادهسازی استандарدهای مستندسازی در لابراتوار دندانسازی لازم نیست یکباره همه چیز را پیچیده کنید؛ کافی است چند دسته سند اصلی را تعریف و برای هر کدام فرم و فرایند مشخص تنظیم کنید.
پرونده هر کیس و اسناد همراه آن
پرونده کیس قلب مستندسازی است. این پرونده – کاغذی یا دیجیتال – باید تصویری کامل از آنچه لابراتوار برای آن بیمار انجام داده ارائه کند. حداقل اطلاعات مهم عبارتاند از:
- مشخصات کدگذاریشده بیمار و نام دندانپزشک
- نوع کار (روکش، بریج، پروتز کامل، ایمپلنت، ارتودنسی و …)
- نسخه یا فرم سفارش کامل، شامل طراحی، ماده، رنگ، تاریخ تحویل
- ایمپرشنها یا فایلهای اسکن، مدلها و تصاویر کلینیکی مرتبط
- سوابق اصلاح، ریمیک، تماسها و تأخیرهای احتمالی
راهنماهای رکوردکیپینگ در دندانپزشکی بر نگهداری نسخههای لابراتواری، ثبت دقیق اقدامات اصلاحی و آرشیو امن این اطلاعات تأکید میکنند.
ردیابی مواد و تجهیزات
یک بخش مهم از استانداردهای مستندسازی در لابراتوار دندانسازی، ردیابی مواد است. برای هر بلوک زیرکونیا، اینگات لیتیومدیسلیکات، رزین پرینتی یا آلیاژ فلزی باید اطلاعات زیر ثبت شود:
- نام تولیدکننده و محصول
- بچنامبر و تاریخ انقضا
- تاریخ ورود و موارد استفادهشده (پیوند به پرونده کیسها)
مقالات مربوط به کیفیت در لابراتوارهای ارتودنسی و ایمپلنتی تأکید میکنند که ردیابی کامل مواد پایه تمام بازرسیهای کیفیت و ایمنی است؛ بدون آن حتی بهترین QC هم اعتبار کافی ندارد
برای تجهیزات نیز باید سوابق سرویس، کالیبراسیون، خرابی و تعمیرات نگهداری شود تا اگر مشکلی در دقت یا کیفیت پیش آمد، بتوان نقش دستگاه را بررسی کرد.
سوابق کنترلکیفی، شکایات و اقدامات اصلاحی
هر مرحله مهم تولید – از طراحی CAD تا میلینگ، پرینت، لایهگذاری و فینیشینگ – باید نقطه کنترلکیفی داشته باشد و نتیجه آن در فرمهای مشخص ثبت شود. این سوابق شامل وضعیت فیت روی دای، تماسهای پروگزیمال، اکلوژن، رنگ و بافت سطحی است.
در کنار آن، سیستم ثبت شکایات دندانپزشک، ریمیکها و اقدامات اصلاحی و پیشگیرانه (CAPA) باید تعریف شود. این اطلاعات در کنار هم، تصویری روشن از عملکرد لابراتوار و اثربخشی کنترلکیفی و نهاییسازی (QC) ارائه میکنند.
ارتباط استانداردهای مستندسازی با کنترل کیفی و نهاییسازی (QC)
اگر مستندسازی و QC دو مسیر جدا از هم باشند، بخش بزرگی از ظرفیت هر دو از بین میرود. هدف این است که استانداردهای مستندسازی در لابراتوار دندانسازی دقیقا همان دادههایی را تولید کنند که در مرحله کنترلکیفی به آن نیاز دارید.
در یک ساختار حرفهای، فرم QC نهایی بخشی از پرونده کیس است و مواردی مثل فیت، اکلوژن، رنگ و مطابقت با نسخه دندانپزشک را بهصورت چکلیست ثبت میکند. همین فرم بعدا در صورت ریمیک یا شکایت، مرجع تحلیل علت ریشهای خواهد بود.
برای طراحی دقیق نقشها، فرمها، چکلیستها و مسیر تأیید نهایی، استفاده از چارچوبهای مطرح در مقاله جامع کنترل کیفی و نهاییسازی (QC) میتواند کمک کند مستندسازی و QC کاملا همگرا شوند، نه اینکه بهصورت جزیرهای اجرا شوند. (( مقاله جامع کنترل کیفی و نهاییسازی (QC) )) در عمل، هر چکلیست QC تبدیل به یک سند رسمی در پرونده فنی پروتز خواهد شد.
پیادهسازی سیستم مستندسازی استاندارد در لابراتوار دندانسازی
اجرای استانداردهای مستندسازی در لابراتوار دندانسازی حتما لازم نیست با نرمافزارهای پیچیده شروع شود؛ مهم این است که ساختار روشن و پایدار باشد.
در مراحل اولیه میتوانید:
- برای هر نوع کار (ثابت، متحرک، ایمپلنتی) فرم استاندارد پذیرش و نسخه طراحی کنید
- لاگ سادهای برای مواد و بچنامبرها بسازید و آن را به کیسها لینک کنید
- فرم کوتاهی برای QC نهایی تعریف کنید که تکمیل آن شرط خروج کار از لابراتوار باشد
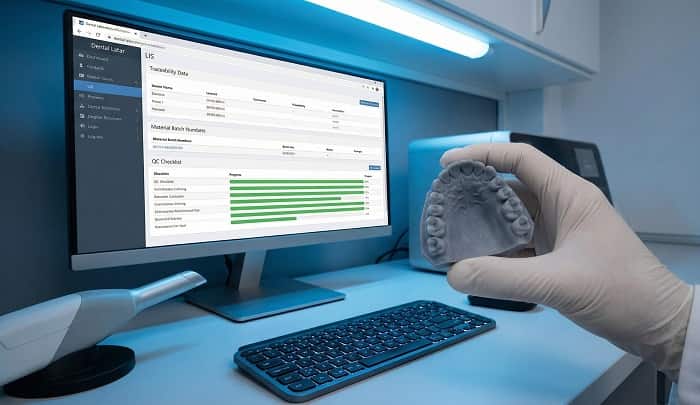
در گام بعد، استفاده از سیستمهای دیجیتال مدیریت لابراتوار یا LIS، امکان اتصال پروندهها، عکسها، فایلهای اسکن و فرمهای QC را در یک پلتفرم واحد فراهم میکند. این کار جستوجو، گزارشگیری و پاسخگویی در برابر ممیزیهای داخلی و خارجی را بسیار ساده میکند
نکته مهم دیگر، آموزش تیم است. تکنسینها باید بدانند چرا این مستندات مهم هستند و چطور کیفیت کار خودشان در آینده به همین دادهها وابسته خواهد بود. اینجاست که میتوانید از توصیههای مرتبط با آموزش و نقش آن در QC که در مقاله جامع کنترل کیفی و نهاییسازی (QC) مطرح میشود استفاده کنید. (( مقاله جامع کنترل کیفی و نهاییسازی (QC) ))
سخن آخر
در نهایت، کیفیت پروتز فقط به زیبایی و فیت امروز آن خلاصه نمیشود؛ بلکه به این بستگی دارد که اگر فردا سوالی، مشکلی یا بازبینیای مطرح شد، لابراتوار بتواند مسیر ساخت آن را بازسازی و از کار خود دفاع کند. این توانایی بدون استانداردهای مستندسازی در لابراتوار دندانسازی وجود نخواهد داشت.
با تعریف پرونده کیس، ردیابی مواد، سوابق QC، شکایات و اقدامات اصلاحی، و پیوند این اجزا با یک سیستم منسجم کنترلکیفی و نهاییسازی (QC)، میتوانید ریسک خطا را کاهش دهید، ریمیک را کم کنید و اعتماد دندانپزشکان و بیماران را بالا ببرید. برای تبدیل این اصول به فرمها، چکلیستها و روندهای عملی، رجوع به مقاله جامع کنترل کیفی و نهاییسازی (QC) و پیادهسازی نکات آن، منطقیترین گام بعدی برای حرفهایتر شدن لابراتوار شما است. (( مقاله جامع کنترل کیفی و نهاییسازی (QC) ))
سوالات متداول درباره استانداردهای مستندسازی در لابراتوار دندانسازی
۱. چرا مستندسازی استاندارد در لابراتوار تا این حد مهم است؟
چون مستندسازی پایه ردیابی، مدیریت ریسک، پاسخگویی حقوقی و بهبود مستمر است. بدون مدارک منظم، نه میتوانید کیفیت را ثابت کنید، نه میتوانید علت مشکل را دقیق پیدا کنید. بسیاری از استانداردهای بینالمللی مثل ایزو ۱۳۴۸۵ و DAMAS مستندسازی را قلب سیستم کیفیت میدانند
۲. چه تفاوتی بین مستندسازی برای استفاده داخلی و الزامات قانونی مثل MDR وجود دارد؟
مستندسازی داخلی بیشتر روی مدیریت کیفیت، ریمیک و کارایی تمرکز دارد، در حالی که MDR و استانداردهای مشابه، وجود پرونده فنی، اظهارنامه انطباق و اسناد ریسک و عملکرد را از نگاه قانون الزامی میکنند. در عمل، یک سیستم خوب مستندسازی میتواند هر دو نیاز را همزمان پاسخ دهد.
۳. این اسناد باید چقدر نگهداری شوند؟
مدت نگهداری دقیق به قوانین هر کشور بستگی دارد، اما راهنماهای کیفیت توصیه میکنند سوابق کیس، مواد و QC برای چند سال پس از تحویل نگهداری شوند تا در صورت شکایت، بازبینی یا مشکل دیرهنگام، امکان ردیابی وجود داشته باشد. راهنماهای رکوردکیپینگ دندانپزشکی هم روی نگهداری نسخههای لابراتواری تأکید میکنند
۴. آیا بدون نرمافزار تخصصی هم میتوان استانداردهای مستندسازی را اجرا کرد؟
بله، در آغاز میتوان با فرمهای کاغذی یا فایلهای ساده، ساختار مستندسازی را پیاده کرد. مهم، کامل بودن دادهها و ثبات در ثبت آنها است. نرمافزارها زمانی ارزشمندتر میشوند که حجم کیسها بالا برود و نیاز به جستوجو و گزارشگیری سریعتر باشد
۵. چه ارتباطی بین مستندسازی و کاهش ریمیک وجود دارد؟
وقتی برای هر ریمیک علت، مواد، مراحل ساخت و نتایج QC ثبت شده باشد، میتوانید الگوهای خطا را ببینید و آنها را در طراحی، آموزش یا فرایند اصلاح کنید. به این ترتیب، هر ریمیک به یک داده برای بهبود تبدیل میشود، نه یک اتفاق تکراری و مبهم.